Свинец физика. Свинец: история открытия элемента
(первый электрон)
(по Полингу)
Pb←Pb 4+ 0,80 В
| Pb | 82 |
| 207,2 | |
| 4f 14 5d 10 6s 2 6p 2 | |
| Свинец | |
Свинец — элемент главной подгруппы четвёртой группы, шестого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 82. Обозначается символом Pb (лат. Plumbum). Простое вещество свинец (CAS-номер: 7439-92-1) — ковкий, сравнительно легкоплавкий металл серого цвета.
Происхождение слова «свинец» неясно. В большинстве славянских языков (болгарском, сербско-хорватском, чешском, польском) свинец называется оловом. Слово с тем же значением, но похожее по произношению на «свинец», встречается только в языках балтийской группы: švinas (литовский), svins (латышский).
Латинское же plumbum (тоже неясного происхождения) дало английское слово plumber — водопроводчик (когда-то трубы зачеканивали мягким свинцом), и название венецианской тюрьмы со свинцовой крышей — Пьомбе, из которой по некоторым данным ухитрился бежать Казанова. Известен с глубокой древности. Изделия из этого металла (монеты, медальоны) использовались в Древнем Египте, свинцовые водопроводные трубы — в Древнем Риме. Указание на свинец как на определённый металл имеется в Ветхом Завете. Выплавка свинца была первым из известных человеку металлургических процессов. До 1990 г. большое количество свинца использовалось (вместе с сурьмой и оловом) для отливки типографских шрифтов, а также в виде тетраэтилсвинца — для повышения октанового числа моторного топлива.
Нахождение свинца в природе
Получение свинца
Страны — крупнейшие производители свинца (включая вторичный свинец) на 2004 год (по данным ILZSG), в тыс. тонн:
| ЕС | 2200 |
| США | 1498 |
| Китай | 1256 |
| Корея | 219 |
Физические свойства свинца
Свинец имеет довольно низкую теплопроводность, она составляет 35,1 Вт/(м·К) при температуре 0°C. Металл мягкий, легко режется ножом. На поверхности он обычно покрыт более или менее толстой плёнкой оксидов, при разрезании открывается блестящая поверхность, которая на воздухе со временем тускнеет.
Плотность — 11,3415 г/см³ (при 20 °C)
Температура плавления — 327,4 °C
Температура кипения — 1740 °C
Химические свойства свинца
Электронная формула: KLMN5s 2 5p 6 5d 10 6s 2 6p 2 , в соответствии с чем он имеет степени окисления +2 и +4. Свинец не очень активен химически. На металлическом разрезе свинца виден металлический блеск, постепенно исчезающий из-за образования тонкой плёнки РbО.
С кислородом образует ряд соединений Рb2О, РbО, РbО2, Рb2О3, Рb3О4. Без кислорода вода при комнатной температуре не реагирует со свинцом, но при большой температуре получают оксида свинца и водород при взаимодействии свинца и горячего водяного пара.
Оксидам РbО и РbО2 соответствуют амфотерные гидрооксиды Рb(ОН)2 и Рb(ОН)4.
При реакции Mg2Pb и разбавленной HCl получается небольшое количество РbН4. PbH4 — газозообразное вещество без запаха, которое очень легко разлагается на свинец и и водород. При большой температуре галогены образовывают со свинцом соединения вида РbХ2 (X — соответствующий галоген). Все эти соединения мало растворяются в воде. Могут быть получены галогениды и типа РbХ4. Свинец с азотом прямо не реагирует. Азид свинца Pb(N3)2 получают косвенным путём: взаимодействием растворов солей Рb (II) и соли NaN3. Сульфиды свинца можно получить при нагревании серы со свинцом, образуется сульфид PbS. Сульфид получают также пропусканием сероводорода в растворы солей Pb (II). В ряду напряжений Pb стоит левее водорода, но свинец не вытесняет водород из разбавленных HCl и H2SO4, из-за перенапряжения Н2 на Pb, а также на поверхности металла образуются плёнки трудно-растворимых хлорида РbCl2 и сульфата PbSO4, защищающие металл от дальнейшего действия кислот. Концентрированные кислоты типа H2SO4 и НCl при нагревании действуют на Pb и образуют с ним растворимые комплексные соединения состава Pb(HSO4)2 и Н2[РbCl4]. Азотная, а также некоторые органических кислоты (например, лимонная) растворяют свинец с получением солей Рb(II). По растворимости в воде соли свинца делятся на нерастворимые (напрммер, сульфат, карбонат, хромат, фосфат, молибдат и сульфид), малорастворимые (вроде, хлорид и фторид) и растворимые (к примеру,ацетат, нитрат и хлорат свинца). Соли Pb (IV) могут быть получены электролизом сильно подкисленных серной кислотой растворов солей Рb (II). Соли Pb (IV) присоединяют отрицательные ионы с образованием комплексных анионов, например, плюмбатов (РbО3)2- и (РbО4)4-, хлороплюмбатов (РbCl6)2-, гидроксоплюмбатов [Рb(ОН)6]2- и других. Концентрированные растворы едких щелочей при нагревании реагируют с Pb с выделением водорода и гидроксоплюмбитов типа Х2[Рb(ОН)4]. Еион (Ме=>Ме++e)=7,42 эВ.
Основные соединения свинца
Оксиды свинца
Оксиды свинца имеют преимущественно основный или амфотерный характер. Многие из них окрашены в красные, жёлтые, чёрные, коричневые цвета. На фотографии в начале статьи, на поверхности свинцовой отливки, в её центре видны цвета побежалости — это тонкая плёнка оксидов свинца, образовавшаяся из-за окисления горячего металла на воздухе.
Галогениды свинца
Халькогениды свинца
Халькогениды свинца — сульфид свинца, селенид свинца и теллурид свинца — представляют собой кристаллы чёрного цвета, которые являются узкозонными полупроводниками.
Соли свинца
Сульфат свинца
Нитрат свинца
Ацетат свинца
— свинцовый сахар, относится к очень ядовитым веществам. Ацетат свинца, или свинцовый сахар, Pb(CH 3 COO) 2 ·3H 2 O существует в виде бесцветных кристаллов или белого порошка, медленно выветривающегося с потерей гидратной воды. Соединение хорошо растворимо в воде. Оно обладает вяжущим действием, но так как содержит ионы ядовитого свинца, то применяется как наружное в ветеринарии. Ацетат применяют также в аналитической химии, крашении, ситценабивном деле, как наполнитель шёлка и для получения других соединений свинца. Основной ацетат свинца Pb(CH 3 COO) 2 ·Pb(OH) 2 — менее растворимый в воде белый порошок — используется для обесцвечивания органических растворов и очистки растворов сахара перед анализом.
Применение свинца
Свинец в народном хозяйстве
Нитрат свинца применяется для производства мощных смесевых взрывчатых веществ. Азид свинца применяется как наиболее широкоупотребляемый детонатор (инициирующее взрывчатое вещество). Перхлорат свинца используется для приготовления тяжелой жидкости (плотность 2,6 г/см³), используемой во флотационном обогащении руд, он иногда применяется в мощных смесевых взрывчатых веществах как окислитель. Фторид свинца самостоятельно, а так же совместно с фторидом висмута, меди, серебра применяется в качестве катодного материала в химических источниках тока. Висмутат свинца, сульфид свинца PbS, иодид свинца применяются в качестве катодного материала в литиевых аккумуляторных батареях. Хлорид свинца PbCl2 в качестве катодного материала в резервных источниках тока. Теллурид свинца PbTe широко применяется в качестве термоэлектрического материала (термо-э.д.с 350 мкВ/К), самый широкоприменяемый материал в производстве термоэлектрогенераторов и термоэлектрических холодильников. Двуокись свинца PbO2 широко применяется не только в свинцовом аккумуляторе, но так же на её основе производятся многие резервные химические источники тока, например — свинцово-хлорный элемент, свинцово-плавиковый элемент и др.
Свинцовые белила , основной карбонат Pb(OH)2.PbCO3, плотный белый порошок, — получается из свинца на воздухе под действием углекислого газа и уксусной кислоты. Использование свинцовых белил в качестве красящего пигмента теперь не так распространено, как ранее, из-за их разложения под действием сероводорода H2S. Свинцовые белила применяют также для производства шпатлевки, в технологии цемента и свинцовокарбонатной бумаги.
Арсенат и арсенит свинца применяют в технологии инсектицидов для уничтожения насекомых — вредителей сельского хозяйства (непарного шелкопряда и хлопкового долгоносика). Борат свинца Pb(BO2)2·H2O, нерастворимый белый порошок, используют для сушки картин и лаков, а вместе с другими металлами — в качестве покрытий стекла и фарфора. Хлорид свинца PbCl2, белый кристаллический порошок, растворим в горячей воде, растворах других хлоридов и особенно хлорида аммония NH4Cl. Его применяют для приготовления мазей при обработке опухолей.
Хромат свинца PbCrO4 известен как хромовый желтый краситель, является важным пигментом для приготовления красок, для окраски фарфора и тканей. В промышленности хромат применяют в основном в производстве желтых пигментов. Нитрат свинца Pb(NO3)2 — белое кристаллическое вещество, хорошо растворимое в воде. Это вяжущее ограниченного применения. В промышленности его используют в спичечном производстве, крашении и набивке текстиля, окраске рогов и гравировке. Сульфат свинца Pb(SO4)2, нерастворимый в воде белый порошок, применяют как пигмент в аккумуляторах, литографии, в технологии набивных тканей.
Сульфид свинца PbS, чёрный нерастворимый в воде порошок, используют при обжиге глиняной посуды и для обнаружения ионов свинца.
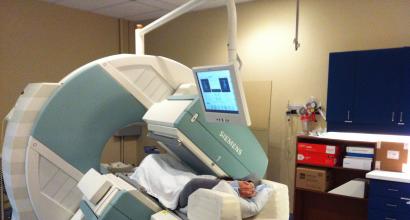
Поскольку свинец хорошо поглощает γ-излучение, он используется для радиационной защиты в рентгеновских установках и в ядерных реакторах. Кроме того, свинец рассматривается в качестве теплоносителя в проектах перспективных ядерных реакторов на быстрых нейтронах.
Значительное применение находят сплавы свинца. Пьютер (сплав олова со свинцом), содержащий 85-90 % Sn и 15-10 % Pb, формуется, недорог и используется в производстве домашней утвари. Припой, содержащий 67 % Pb и 33 % Sn, применяют в электротехнике. Сплавы свинца с сурьмой используют в производстве пуль и типографского шрифта, а сплавы свинца, сурьмы и олова — для фигурного литья и подшипников. Сплавы свинца с сурьмой обычно применяют для оболочек кабелей и пластин электрических аккумуляторов. Соединения свинца используются в производстве красителей, красок, инсектицидов, стеклянных изделий и как добавки к бензину в виде тетраэтилсвинца (C2H5)4Pb (умеренно летучая жидкость, пары к-рой в малых концентрациях имеют сладковатый фруктовый запах, в больших-неприятный запах; Тпл = 130 °C, Ткип = 80°С/13 мм рт.ст.; плотн. 1,650 г/см³; nD2v = 1,5198; не раств. в воде, смешивается с орг. растворителями; высокотоксичен, легко проникает через кожу; ПДК = 0,005 мг/м³; ЛД50 = 12,7 мг/кг (крысы, перорально)) для повышения октанового числа.
Свинец в медицине
Экономические показатели
Цены на свинец в слитках (марка С1) в 2006 году составили в среднем 1,3—1,5 долл/кг.
Страны, крупнейшие потребители свинца в 2004 году, в тыс. тонн (по данным ILZSG):
| Китай | 1770 |
| ЕС | 1553 |
| США | 1273 |
| Корея | 286 |
Физиологическое действие
Свинец и его соединения токсичны. Попадая в организм, свинец накапливается в костях, вызывая их разрушение. ПДК в атмосферном воздухе соединений свинца 0,003 мг/м³, в воде 0,03 мг/л, почве 20,0 мг/кг. Выброс свинца в Мировой океан 430—650 тысяч т/год.
Свойства свинца
Существует не только свекольный или тростниковый , но и свинцовый. Так называют одно из соединений металла.
Ацетат выглядит как сладкая добавка к пище, — мелкие белого цвета или порошок, хорошо растворимый в воде.
Однако, свинцовый сахар не сладкий, да и есть его, не рекомендуется. Вещество содержит яд, коим являются как раз ионы металла.
Применяют ацетат только в ветеринарии исключительно наружно, поскольку обладает вяжущими свойствами.
Ядовитость некоторых соединений свинца, как это ни странно, используется во благо человека, но не насекомых.
Вещество под названием арсенат, содержащее металл, — отрава для вредителей полей, таких как долгоносик хлопковый и непарный шелкопряд.
Есть целый спектр и безобидных сочетаний свинца с другими элементами.
В сочетании с металл обладает сушащими свойствами, веществом обрабатывают картины, чтобы краска быстрее запустевала.

— Хромат свинца солнечного цвета. Его применяют для окрашивания тканей, .
— Без сульфата металла не обходятся аккумуляторы.
— Тетраэтилсвинец служит добавкой к машинному топливу, улучшает качественные параметры .
— Без сульфида металла не возможен обжиг посуды и изделий из .
— Хлорид свинца замедляет рост опухолей, поэтому используется медиками в качестве мази.
Это, применение химических соединений свинца . В чистом же виде элемент пригождается в промышленности.
Применение свинца
Металл не благородный, зато, помогает получить драгоценные и в их чистом виде. Процесс называется купелирование.
В процессе плавления смеси и свинца под воздействием окисления, отделяется драгоценный металл без каких-либо примесей.
Добавляют свинец и в смеси, которые употребляют в качестве припоев.
Их применяют для спаивания между собой деталей . Сам по себе свинец не отличается эстетической красотой.

Не соприкасаясь с воздухом, он блестящий, бело-голубой. Но, стоит металлу прореагировать с кислородом в атмосфере, как он теряет лоск, покрывается непрозрачной, мутной пленкой. Так что, с эстетической точки зрения свинец не представляет ценности.
Зато, элемент под порядковым номером 82 в – герой многих литературных трудов. Писатели любят эпитет «свинцовый».
Обычно, он означает неимоверную тяжесть чего-либо. К примеру, фраза «свинцовые ноги » трактуется, как конечности, которыми невозможно передвигать из-за ощущения в них тяжести.
Металл №82, действительно, не легок, но далеко не самый тяжелый из известных веществ. К примеру, в кусочек свинца плавает на поверхности.
Так что, более точно другое литературное применение образа элемента. Понятие «свинцовый» употребляют по отношению к цвету.
Часто говорят «свинцовый цвет лица». Это значит что покровы нездоровой серо-синей окраски, такой, какую металл приобретает при соприкосновении с воздухом.
В переводе некоторых текстов можно встретить фразу «оловянные аккумуляторы».
Это издержки перевода текстов на литовском, латышском, болгарском языках не совсем компетентными людьми.

Дело в том, что слова свинец во многих странах просто нет. Этот элемент называют оловом.
Еще древние люди путали два похожих друг на друга металла. Правда, олово тысячелетия назад не удостоилось чести представлять какую-нибудь планету.
Другие металлы, известные с незапамятных времен, древние люди разделили по небесным телам. Не секрет, что символизировало Марс. Свинец же стал обозначать Сатурн.
82-ым элементом буквально напичкана земля и, это касается не только природных запасов металла, но и коммуникационных систем.
Свойства свинца спасают от коррозии линии электропередач, телеграфные провода. Их часто приходится прокладывать не по воздуху, а под водоемами или, просто, под землей.
Не обходятся без бело-голубого металла и водопроводные системы. В них элемент свинец – материал для запорных устройств. Они препятствуют незапланированному доступу, в коллекторы, к примеру.
Количество свинца во внешней среде влияет на уровень преступности. К такому выводу пришли ученые США.
Они обследовали все штаты страны, соотнесли цифры и выявили закономерность.
Там, где концентрация металл максимальна, совершается в 4 раза больше правонарушений, чем в областях с меньшими показателями элемента №82.
Ученые мужи даже нашли объяснение статистическим данным. Они предположили, что металл свинец способствует нарушению нейронных связей в мозге, разрушает некоторые химические соединения, необходимые для нормальной работы органа.
Возможно, это способствует перепрограммированию человека на более нестандартное и агрессивное поведение.
Кстати, свинец в истории человечества часто был связан именно с агрессией. Металл применяли в пытках.

Лили в расплавленном виде на кожные покровы, рот. В индии сплав заливали в уши представителям низшей касты, если те подслушали разговоры своих высших собратьев.
А в Венеции для опасных преступников делали свинцовые потолки камер на верхнем этаже тюрьмы.
В жару они раскалялись, — узники изнывали от температур и духоты. В прохладную погоду, напротив, в помещениях было очень холодно.
Но, к счастью, сейчас металл №82 используют, в основном, в благих целях. Основной добытчик свинца – КНР.
В Поднебесной добывают около 2-х миллионов тонн элемента в год. Для сравнения, все запасы России равны лишь 17-ти миллионам тонн. Большинство из них скрыты в недрах Приморского, Алтайского, Красноярского краев.
Свинец обычно имеет грязно-серый цвет, хотя свежий его разрез имеет синеватый отлив и блестит. Однако блестящий металл быстро покрывается тускло-серой защитной пленкой оксида. Плотность свинца (11,34 г/см3) в полтора раза больше, чем у железа, вчетверо больше, чем у алюминия; даже серебро легче свинца. Свинец очень легко плавится – при 327,5° С, кипит при 1751° С и заметно летуч уже при 700° С. Этот факт очень важен для работающих на комбинатах по добыче и переработке свинца. Свинец – один из самых мягких металлов. Он легко царапается ногтем и прокатывается в очень тонкие листы. Свинец сплавляется со многими металлами. С ртутью он дает амальгаму, которая при небольшом содержании свинца жидкая.
Свинец кристаллизуется в гранецентрированной кубической решётке (а = 4,9389), аллотропических модификаций не имеет. Атомный радиус 1,75, ионные радиусы: Pb 2+ 1,26 , Pb 4+ 0,76: плотность 11,34 г/см 3 (20°C); удельная теплоёмкость при 20°C 0,128 кДж/(кг·К) ; теплопроводность 33,5 вт/(м·К); температурный коэффициент линейного расширения 29,1·10 -6 при комнатной температуре; твёрдость по Бринеллю 25-40 Мн/м 2 (2,5-4 кгс/мм 2); предел прочности при растяжении 12-13 Мн/м 2 , при сжатии около 50 Мн/м 2 ; относительное удлинение при разрыве 50-70%. Наклёп не повышает механических свойств свинца, т. к. температура его рекристаллизации лежит ниже комнатной (около -35 °C при степени деформации 40% и выше). Свинец диамагнитен, его магнитная восприимчивость - 0,12·10 -6 . При 7,18 К становится сверхпроводником.
Относительная атомная масса (A r = 207,2) является усредненной из масс нескольких изотопов: 204 Pb (1,4%), 206 Pb (24,1%), 207 Pb (22,1%) и 208 Pb (52,4%). Последние три нуклида – конечные продукты естественных радиоактивных превращений урана, актиния и тория. Известно также более 20 радиоактивных изотопов свинца, из которых наиболее долгоживущие – 202 Pb и 205 Pb (с периодами полураспада 300 тысяч и 15 млн. лет). В природе образуются также и короткоживущие изотопы свинца с массовыми числами 209, 210, 212 и 214 с периодами полураспада соответственно 3,25 ч, 27,1 года, 10,64 ч и 26,8 мин. Соотношение различных изотопов в разных образцах свинцовых руд может несколько различаться, что не дает возможности определить для свинца значение A r с большей точностью.
ОПРЕДЕЛЕНИЕ
Свинец - восемьдесят второй элемент Периодической таблицы. Обозначение - Pb от латинского «plumbum». Расположен в шестом периоде, IVA группе. Относится к металлам. Заряд ядра равен 82.
Свинец - голубовато-белый тяжелый металл (рис. 1). В разрезе поверхность свинца блестит. На воздухе покрывается пленкой оксидов и из-за этого тускнеет. Он очень мягок и режется ножом. Обладает низкой теплопроводностью. Плотность 11,34 г/см 3 . Температура плавления 327,46 o С, кипения 1749 o С.
Рис. 1. Свинец. Внешний вид.
Атомная и молекулярная масса свинца
Относительной молекулярная масса вещества (M r) - это число, показывающее, во сколько раз масса данной молекулы больше 1/12 массы атома углерода, а относительная атомная масса элемента (A r) — во сколько раз средняя масса атомов химического элемента больше 1/12 массы атома углерода.
Поскольку в свободном состоянии свинец существует в виде одноатомных молекул Pb, значения его атомной и молекулярной масс совпадают. Они равны 207,2.
Изотопы свинца
Известно, что в природе свинец может находиться в виде четырех стабильных изотопов 204 Pb, 206 Pb, 207 Pb и 208 Pb. Их массовые числа равны 204, 206, 207 и 208 соответственно. Ядро атома изотопа свинца 204 Pb содержит восемьдесят два протона и сто двадцать два нейтрона, а остальные отличаются от него только числом нейтронов.
Существуют искусственные нестабильные изотопы свинца с массовыми числами от 178-ми до 215-ти, а также более десяти изомерных состояний ядер, среди которых наиболее долгоживущими являются изотопы 202 Pb и 205 Pb, периоды полураспада которых равны 52,5 тысячи и 15,3 млн. лет соответственно.
Ионы свинца
На внешнем энергетическом уровне атома свинца имеется четыре электрона, которые являются валентными:
1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5р 6 5d 10 6s 2 6р 2 .
В результате химического взаимодействия свинец отдает свои валентные электроны, т.е. является их донором, и превращается в положительно заряженный ион:
Pb 0 -2e → Pb 2+ ;
Pb 0 -4e → Pb 4+ .
Молекула и атом свинца
В свободном состоянии свинец существует в виде одноатомных молекул Pb. Приведем некоторые свойства, характеризующие атом и молекулу свинца:
Примеры решения задач
ПРИМЕР 1
ПРИМЕР 2
| Задание | К раствору нитрата свинца (II) массой 80г (массовая доля соли 6,6%) прилили раствор йодида натрия массой 60 г (массовая доля NaI 5%). Рассчитайте массу йодида свинца (II), выпадающего в осадок. |
| Решение | Запишем уравнение реакции взаимодействия нитрата свинца (II) с иодидом натрия:
Pb(NO 3) 2 + 2NaI = PbI 2 ↓ + 2NaNO 3 . Найдем массы растворенных веществ нитрата свинца (II) и иодидом натрия: ω = m solute / m solution × 100%; m solute = ω /100%×m solution ; m solute (Pb(NO 3) 2)=ω(Pb(NO 3) 2) /100%×m solution (Pb(NO 3) 2); m solute (Pb(NO 3) 2) = 6,6 /100%× 80 = 5,28 г; m solute (NaI) = ω (NaI) /100%×m solution (NaI); m solute (NaI) =5 /100% × 60 = 3 г. Найдем количество моль веществ, вступивших в реакцию (молярная масса нитрата свинца (II) равна 331 г/моль, иодида натрия - 150 г/моль) и определим, какое из них находится в избытке: n(Pb(NO 3) 2) =m solute (Pb(NO 3) 2) / M (Pb(NO 3) 2); n (Pb(NO 3) 2) = 5,28 / 331 = 0,016моль. n(NaI) =m solute (NaI) / M (NaI); n (NaI) = 3 / 150 = 0,02 моль. Иодид натрия находится в избытке, следовательно, все дальнейшие расчеты ведем по нитрату свинца (II). n (Pb(NO 3) 2) : n (PbI 2) = 1:1, т.е. n (Pb(NO 3) 2) = n (PbI 2) = 0,016 моль. Тогда масса иодида свинца (II) будет равна (молярная масса - 461 г/моль): m (PbI 2) = n (PbI 2) × M (PbI 2); m (PbI 2) = 0,016 × 461 = 7,376 г. |
| Ответ | Масса иодида свинца (II) равна 7,376 г. |
Восемьдесят второй элемент таблицы Менделеева людям знаком давно. Скифские шаманы в обязательном порядке нашивали на ритуальную одежду свинцовые пластинки и бусины, «чтобы не улететь безвозвратно в мир духов». В египетских захоронениях обнаружены фигурки из свинца, датируемые VI веком до нашей эры. Но особым почтением к свинцу отличались древние римляне – там из него делали водопроводы, крыши, посуду для вина, и много еще чего. Их опыт попытались перенять строители Московского кремля, но, увы (или может быть, к счастью, учитывая влияние свинца на человека) первый же пожар уничтожил их труды...
Подробный экскурс в историю займет не одну страницу, поэтому разумнее посвятить ему отдельную статью.
Применение и свойства
Звездный час свинца настал с изобретением огнестрельного оружия. Но этот металл годится не только на пули и дробь. Без него встал бы абсолютно весь транспорт, ведь он – элемент автомобильных аккумуляторов, которые так и называются: свинцово-кислотные. Бокалы за праздничным столом звенели бы не так благозвучно – свинец входит в состав хрусталя (хотя впервые он попал туда по ошибке одного чешского стеклодува). Рентгеновские кабинеты прекратили бы прием пациентов – от радиации ничто не защищает, кроме свинцовых фартуков. А чем бы мы паяли? И еще много, много всего не удалось бы сделать, если бы в арсенале человечества не было тяжелого серого металла. Да, кстати, про арсеналы: нитрат свинца используется для производства мощной взрывчатки, а в качестве детонатора наиболее распространен азид свинца.
«Серебристо-белый металл с голубоватым отливом, блестящий на срезе»… Так говорит про свинец Википедия. Многих это описание приведет в недоумение, ведь цвет свинца всем известен – он серо-черный, как низкие грозовые тучи. А все потому, что на воздухе происходит стремительное окисление свинца, а пленка окислов придает поверхности металла темный оттенок.
В детстве многие самостоятельно изготавливали свинцовые грузила для рыбалки. Нужно насыпать в консервную банку «потроха» от старых аккумуляторов и совсем недолго нагреть плошку на костре. Температура плавления свинца всего 328 градусов по Цельсию. Затем вылить расплавленный металл на плоский камень… готово, можно резать. Для этого не нужны особые усилия – подойдет обычный нож и даже старые ножницы. Plumbum – мягкий металл, его пластинки можно без усилий свернуть в трубочку.

Фото: Свинец очень удобно использовать в качестве рыболовных грузил -
он не подвержен коррозии, легко принимает нужную форму.
Что тяжелее свинца? Из тех веществ, которые можно встретить в быту, прямо скажем, немногие. Золото – оно тяжелее свинца почти в два раза. И ртуть. Если кусок свинца положить в емкость с ртутью, он будет плавать на поверхности.
Расплавленный свинец напоминает ртуть – он блестящий, подвижный, и в нем, как в зеркале, отражаются окружающие предметы. Но, остывая, свинец тут же окисляется и покрывается мутной пленкой, темнеющей на глазах. Если вылить каплю расплавленного свинца в воду, то получатся всякие замысловатые фигурки, не хуже иных творений модных скульпторов. Но не рекомендуем увлекаться подобным творчеством – свинец ядовит, хотя влияние его на человека проявляется далеко не сразу. Особенно коварны его пары. Тот, кто работает со свинцом, должен регулярно проходить медицинские осмотры.
Ученые из США на протяжении многих лет собирали статистику, которая подтвердила, что в тех районах, где ведется добыча и переработка свинца, уровень преступности в 4 раза превышает аналогичные показатели в среднем по стране.
От автора: российским ученым стоит провести встречный эксперимент и поразить коллег из США сенсационными данными: в районах, где ведется добыча свинца открытым способом, похмелье переносится в 4 раза легче, чем в среднем по стране…
Месторождения свинца
Свинец в природе в чистом виде не встречается. Он всегда смешан с каким-либо металлом, чаще всего с оловом и сурьмой. Обязательно содержится в урановых и ториевых рудах, потому что свинец – не что иное, как последняя стадия распада урана. Вернее, в природе существует пять стабильных изотопов свинца, из которых три – продукты распада U и Th. Эти три изотопа занимают 98,5% от всего количества Pb, содержащегося в земной коре. В процессе ядерной реакции возникают и тут же распадаются многочисленные радиоактивные изотопы свинца.
Основным сырьем для получения свинца служит галенит, он же - свинцовый блеск, химическая формула - PbS. Его кристаллы тяжелые, блестящие и хрупкие.

Фото: Галенит или свинцовый блеск, PbS
Минералы, содержащие свинец и цинк (а также серебро, медь, железо, кадмий и ряд других металлов) образуют общее рудное тело. Комплексные полиметаллические руды имеют в составе такие ценные элементы, как золото, галлий, индий и многие другие. В настоящее время наиболее экономически выгодно извлекать из них свинец и цинк, реже – серебро. Остальное складируют под открытым небом в так называемые хвостохранилища. Это не отходы, а резервы сырья. В перспективе возможна их повторная отработка.
Состав руд Горевского месторождения уникален в своем роде:
(Продолжение следует...)